
第二十一届全国临床肿瘤学(CSCO)大会于2018年9月20日在厦门隆重召开,大会精彩纷呈, PD-1/L1药物当仁不让成为各会场的热点,除免疫治疗的疗效和临床实践话题,PD-L1等伴随诊断的发展和应用也进行了多方位的讨论,精准治疗,伴随诊断先行。
免疫治疗逐渐从配角变成主角,改变了肿瘤传统手术治疗、放化疗的格局,改变了临床实践。其中通过FDA批准上市的PD-1/L1抑制剂有百时美施贵宝的纳武单抗、默沙东的帕博利珠单抗、罗氏的Tecentrip、阿斯利康的Imfinzi、默克生产的Bavencio,可应用于多种实体瘤,例如黑色素瘤、肺癌、头颈鳞状细胞癌、霍奇金淋巴瘤等瘤种。国内CFDA获批的PD-L1单抗药物有百时美施贵宝的纳武单抗和默沙东的帕博利珠单抗。国内制药公司如恒瑞、君实、信达、百济神州的PD-1/L1抗体药物也在紧锣密鼓的临床研究中,相信不久也会走进临床。

1. 免疫治疗伴随诊断的发展
1.1 PD-1/L1表达预测药物疗效
NCCN指南中明确提出对于无明确驱动基因突变的晚期NSCLC患者应进行PD-L1检测,筛选可用PD-1抑制剂帕博利珠单抗的患者,PD-L1≥50%时一线使用帕博利珠单抗,PD-L1≥1%时二线使用。这也是目前唯一获批用于一线肺癌的单药免疫疗法。由Keynote-042 的结果可看到,较化疗方案,整体PD-L1 ≥1% 的NSCLC 患者可从帕博利珠单抗单药的一线治疗获益,整体死亡风险比显着下降。PD-L1 表达量越高, 帕博利珠单抗单药治疗获益越显着。纳武单抗在治疗非肺鳞癌的患者中,PD-L1表达水平临界值以上具有更好的临床获益(TPS为1%/5%/10%时均有更好的OS);HNSCC和尿路上皮癌患者中,PD-L1阳性表达(TPS≥1%)的患者有更好的临床获益。Atezolizumab在治疗尿路上皮癌中,以肿瘤浸润淋巴细胞(IC%)所占比例评级,5%为临界值,临界值以上具有更好的临床获益(ORR)。
1.2 肿瘤突变负荷(TMB)与免疫治疗
Checkmate-032研究是一项一线治疗失败的晚期小细胞肺癌的I/II期临床试验,分为纳武单抗治疗组和纳武单抗联合CTLA-4抗体Ipilimumab治疗组。高TMB患者接受双药联合治疗后ORR为 46%,而中低TMB的患者治疗后的ORR率分别为 16%、22%;单药治疗的肿瘤突变高、中、低负荷的患者的ORR分别为 21%、7%、5%。高TMB患者接受双药联合治疗的一年OS比例为 62%,而中低TMB患者则分别为 20%、23%。CheckMate -227研究结果也显示,TMB作为一种重要的、独立的预测性生物标志物,可以鉴别出那些可能在纳武单抗联合Ipilimumab一线治疗中获益的NSCLC患者。
1.3 MSI-H/dMMR检测与PD-1/L1单抗治疗
2017年5月美国FDA首次批准依靠生物标志物MSI/MMR来进行选择治疗方案,不以肿瘤部位为参考。FDA批准了PD-1抗体帕博利珠单抗用于高度微卫星不稳定性(MSI-H)或错配修复基因缺陷(dMMR)的不可切除的或转移性实体肿瘤患者。同年8月,FDA又批准了纳武单抗在MSI-H或dMMR结直肠癌中的相似适应证。携带MSI-H/dMMR变异的肿瘤分布广泛,在结直肠癌、子宫内膜癌、胃癌、肝细胞癌、壶腹癌、甲状腺癌、皮肤癌、卵巢癌、子宫颈癌、食管腺癌等癌种中均有出现。上述MSI-H/dMMR的肿瘤患者均有可能从免疫治疗中获益,在免疫治疗的优势人群筛选中具有重要价值。
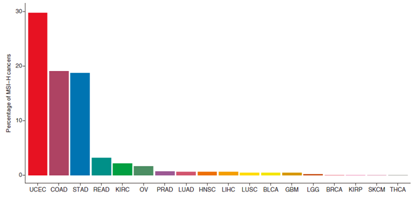
1.4 TMB与PD-L1检测
一篇Nature Medicine文章对POPLAR和OAK样本进行回顾性分析,对比组织tTMB和血液bTMB一致性,并分析bTMB与PD-L1表达的相关性。结果显示组织样本与血样本bTMB结果阳性一致率百分比为64%,阴性一致率百分比为88%;bTMB和PD-L1的表达不相关,均属于独立预测因子。但研究但同时也看到bTMB≥且PD-L1高表达的患者疗效更佳。
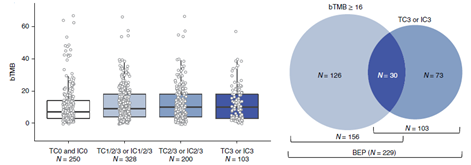
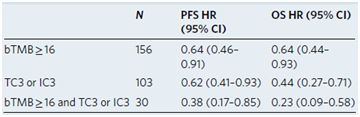
Keynote的系列(010,024,042等)研究中已经证明PD-L1能够有效筛选帕博利珠单抗优势人群,并且Dako PD-L1 IHC 22C3 pharmDx 也获得 FDA 认证作为默沙东帕博利珠单抗的伴随诊断试剂,用于PD-L1高表达人群一、二线治疗。Checkmate-026的研究显示,对比含铂两药化疗,晚期NSCLC一线使用纳武单抗治疗在PD-L1≥5%/50%的腺癌患者中两者PFS没有显著性差异。但在随后的回顾性研究中发现,采用TMB作为标志物对,能更好地区分获益人群。在TMB高表达的病人中,纳武单抗的ORR为47%和PFS为9.7月结果显着优于化疗。Checkmate 227研究采用了2个Biomarker PD-L1和TMB,结果显示无论PD-L1表达状态,对于TMB≥10 mut/Mb患者,纳武单抗联合化疗的ORR和PFS显著优于单纯化疗,TMB状态为纳武单抗的联合治疗提供了有效的Biomarker,双IO联合为高TMB患者提供了持久的临床疗效。
上述研究表明,PD-L1和TMB是PD-L1抑制剂药物疗效独立的预测指标,两个方案检测的人群不重叠(少部分),单独检测TMB会漏掉一部分患者,失去使用免疫治疗的机会。两种方法可相互补充,让更多的患者获益。
1.5 Biomarker的选择
目前PD-1/L1药物已经进入临床,但其配套的伴随诊断试剂尚未实现标准化。PD-L1、TMB、MSI的检测三足鼎立,特别是各个公司的TMB检测标准还不统一,检测结果准确性有待验证。如何选取合适的biomarker是摆在临床实践中一个重要问题。通过上述研究的梳理,我们可以看到对于帕博利珠单抗,应当遵循相关临床指南,NSCLC一线使用首先判断PD-L1表达是否大于50%,后线使用检测表达是否大于1%。对于PD-L1表达未达表达限值,可以考虑MSI/MMR检测,筛选微卫星不稳定性患者。TMB对于欲使用纳武单抗的患者是一个有价值的biomarker,而PD-L1表达也是重要的参考值,PD-L1高表达也有较好的临床获益。PD-L1表达、肿瘤负荷TMB和MSI不稳定性都是预测免疫疗效的重要指标,更多的标志物如新抗原、EBV等也在临床研究中得到肯定。但到目前为止还没有一种适用所有PD-1/L1药物的精准标志物。
多标志物联合检测、相互补充可给更多患者接受免疫治疗的机会,但先后次序很重要。根据目前的指南推荐、临床实践和患者的经济性,PD-L1检测是首选,例如≥50%的患者可一线使用帕博利珠单抗,≥1%二线使用;而PD-L1表达高的患者从阿特珠单抗/纳武单抗中得到更多临床获益。其次是TMB检测,TMB大于10 mut/ mb的患者推荐纳武单抗等药物。而MSI也是重要的备选检测指标。
2 选择可靠的PD-L1检测
数问生物在国内率先推出首个原创的PD-L1检测试剂盒,与国际上(美国FDA)获批产品Dako 22C3相比有良好的一致性。通过对327例的NSCLC临床样本检测,数问生物PD-L1检测与Dako 22C3试剂盒高度的阳性一致性为95.56%,阴性一致性为97.87%,总体一致性为97.55%。体现了数问生物PD-L1试剂的高品质和可靠的检测能力。
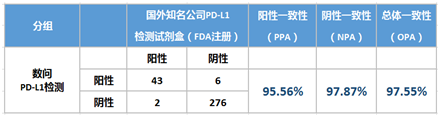
数问生物PD-L1检测优势在恒瑞领先药物SHR1210的临床试验中得到验证,该项多中心研究显示在治疗常规化疗失败或不能耐受的晚期消化道肿瘤食管癌中,采用数问生物PD-L1检测的高表达晚期食管鳞癌患者可从恒瑞抗PD-1药物SHR1210获益,PD-L1阳性(PD-L1表达≥5%)患者具有更高的客观缓解率。数问旗下数问观止检验中心获得美国病理学家协会CAP认证且通过PD-L1的室间质评,可为临床提供优秀的检测结果和重要参考。
3. 参考文献
1.Wu YL, et al. AACR 2018; Abstract CT114.
2.ClaudiaAllemani, et al. The Lancet, 2018, 391(10125) :1023-1075.
3.http://cnda.cfda.gov.cn/WS04/CL2056/228364.html.
4.Lu S, et al. CSCO 2018.Results of CheckMate078.
5.Horn L, et al. J Clin Oncol. 2017 Dec 10;35(35):3924-3933.
6.Brahmer JR, et al,ASCO 2017,Abstract 9000.
7.N Engl J Med 2016;375:1856-67.
8.Nat Med. 2016 Nov;22(11):1342-1350.
9.Nat Med. 2018,24, pages1441–1448
10.Clinical Cancer Research,2018






.png)

